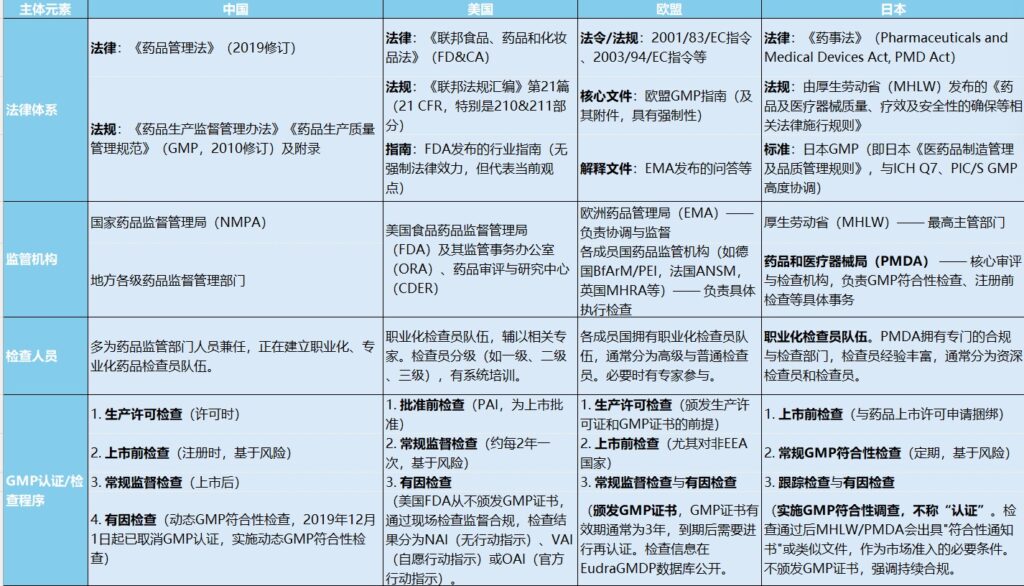
法律体系:从 “强制立法” 到 “多层级规范”
不同经济体的 GMP 法律依据呈现 “强制核心 + 配套细则” 的共性,但具体构成各有侧重:
- 中国:以《药品管理法》(2019 修订)为核心法律,配套《药品生产监督管理办法》《药品生产质量管理规范》(GMP,2010 修订)及附件,形成 “法律 - 法规 - 规范” 的层级体系。
- 美国:依托《联邦食品、药品和化妆品法》(FD&C Act)作为基础法律,以《联邦法规汇编》第 21 篇(21 CFR,尤其是 210、211 部分)为强制法规,FDA 发布的行业指南则作为非强制但具有指导性的补充文件。
- 欧盟:以 2001/83/EC、2003/94/EC 等指令为法律基础,核心执行文件是欧盟 GMP 指南(及附件),同时 EMA 发布的问答类文件作为解释细则,实现区域内监管标准的统一。
- 日本:以《药事法》(PMD Act)为法律框架,由厚生劳动省(MHLW)发布的《药品及医疗器械质量、疗效及安全性确保等相关法律施行规则》为配套法规,日本 GMP(《医药品制造管理及品质管理规则》)则与 ICH Q7、PIC/S GMP 高度协调。
监管机构:“集中统筹” 与 “分散执行” 的协同
各国监管机构均采用 “主管部门 + 执行机构” 的架构,但职责划分有所不同:
- 中国:由国家药品监督管理局(NMPA)统筹全国监管,地方各级药品监管部门负责具体执行,形成 “中央 - 地方” 分级管理模式。
- 美国:以美国食品药品监督管理局(FDA)为核心,其下属的监管事务办公室(ORA)负责现场审计检查、药品审评与研究中心(CDER)负责技术审评,实现 “监管 - 审评” 的职能分离。
- 欧盟:采取 “区域协调 + 成员国执行” 模式 —— 欧洲药品管理局(EMA)负责区域内标准协调与监督,各成员国监管机构(如德国 BfArM/PEI、法国 ANSM、英国 MHRA)承担具体检查工作。
- 日本:厚生劳动省(MHLW)为最高主管部门,药品和医疗器械局(PMDA)作为核心审评与检查机构,直接负责 GMP 符合性检查、注册前检查等实务。
审计检查人员:从 “兼职过渡” 到 “职业化队伍”
检查人员的专业性是 GMP 监管落地的关键,各国队伍建设路径存在差异:
- 中国:目前多为药品监管部门人员兼任,正逐步推进职业化、专业化药品检查员队伍的建设。
- 美国:已建立成熟的职业化检查员队伍,配套专家支持,且检查员实行分级(一级、二级、三级)管理,有系统的培训体系。
- 欧盟:各成员国均配备职业化检查员队伍,通常分为高级与普通检查员,必要时邀请专家参与检查。
- 日本:PMDA 拥有专门的合规与检查部门,检查员经验丰富,分为资深检查员和普通检查员,职业化程度较高。
GMP 认证 / 审计检查程序:“动态合规” 与 “风险导向” 的实践
各国的检查程序均以 “风险管控” 为核心,但认证形式、检查频次有所区别:
- 中国:检查程序包括生产许可检查、上市前检查(基于风险)、常规监督检查,2019 年 12 月起取消 GMP 认证,改为动态 GMP 符合性检查,强化全生命周期监管。
- 美国:不颁发 GMP 证书,通过 “批准前检查(PAI)、常规监督检查(约每 2 年一次)、有因检查” 实现监管,检查结果分为 NAI(无行动指示)、VAI(自愿行动指示)、OAI(官方行动指示)三类。
- 欧盟:需通过生产许可检查(作为 GMP 证书发放前提)、上市前检查(针对非 EEA 国家)、常规及有因检查;GMP 证书有效期通常为 3 年,需定期再认证,检查信息在 EudraGMP 数据库公开。
- 日本:不称 “认证” 而实施 GMP 符合性调查,检查程序包括上市前审计检查(与上市许可绑定)、常规 GMP 符合性审计检查、跟踪及有因审计检查;审计检查通过后发放 “符合性通知书”,不颁发 GMP 证书,强调持续合规。
中国、美国、欧盟、日本的 GMP 监管体系,既体现了 “保障药品质量安全” 的共同目标,也因法律传统、行政架构的差异形成了各具特色的模式。随着 ICH、PIC/S 等国际协调机制的推进,各国监管标准正逐步趋同,但 “职业化队伍建设”“动态合规监管” 仍是全球 GMP 监管的重要发展方向。
中国药企闯日本市场?GMP 合规不迷路!
法玛培明(日本 Pharma Planning)提供《GMP 省令》全文翻译、PMDA 审计翻译 + 专业咨询,懂日本法规更懂中国企业需求,欢迎随时联络!

