笔者:宝田哲仁
第 2 章适用范围已在第一篇中进行了解说,本篇(其二)将进入第 3 章风险评估与风险控制的内容。
图 1 展示了质量风险管理(QRM)的整体框架。本次风险评估的特点,是从化学特性、安全性与质量三者关联性开展评估。QRM 具体步骤将在第三篇及后续内容中详细说明,本篇仅作概述。
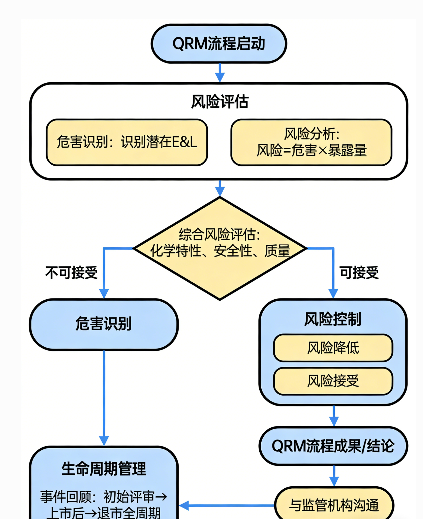
图 2 概括了构建风险矩阵时应考虑的要点。
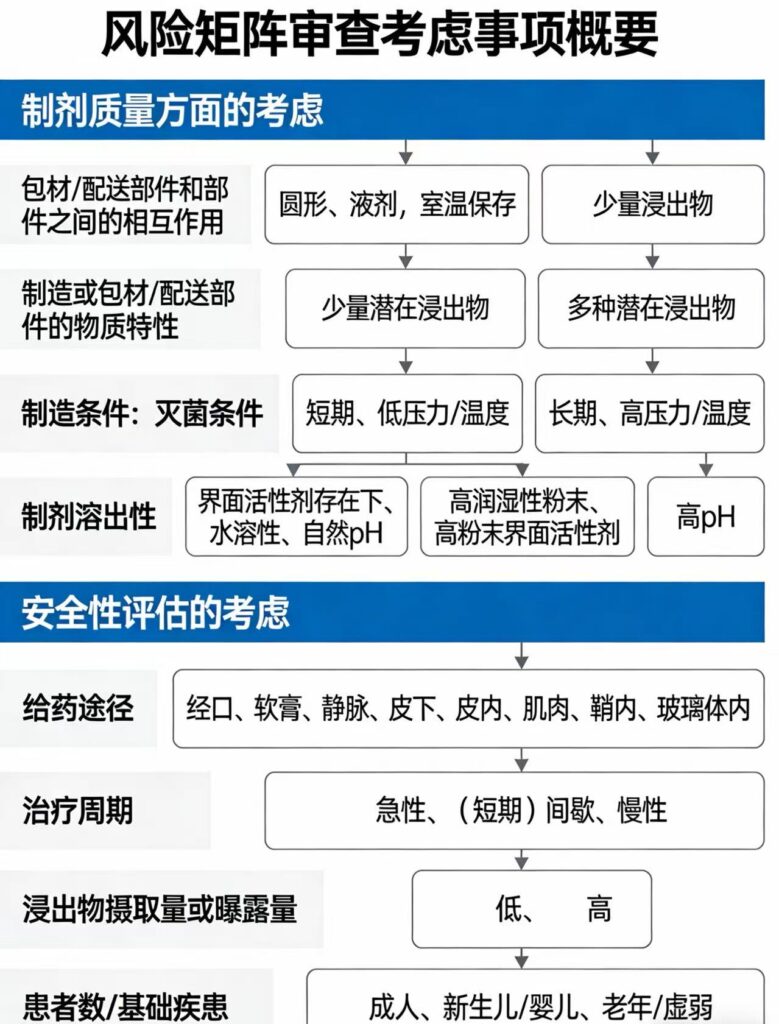
对浸出物实施风险控制,多维度评估至关重要。
一、质量方面的考量要点
・生产设备、包装材料与制剂之间的相互作用
・可能产生浸出物的设备及部件的化学、物理特性,以及使用前的处理方式
・生产条件与贮存条件(表面积与体积比、温度、接触时间、后续工序去除步骤的接近程度 * 及去除能力等)
・制剂的浸出倾向(API、pH、有机共溶剂 **、表面活性剂 / 螯合剂等)
* 去除步骤的接近程度(proximity):应理解为浸出物产生后被去除的快慢程度,需同时考虑空间距离与时间间隔因素。
** 有机共溶剂:指在主溶剂中难以溶解时使用的辅助溶剂。
二、安全性方面的考量要点
需评估浸出物带来的潜在危害性。
评估时需考虑与暴露相关的因素:
给药途径、目标患者人群、给药剂量、给药频率、给药间隔、最长治疗周期
指南指出:
对于口服给药制剂,若能充分论证合理性,可仅符合食品接触安全相关法规即可;
除此以外的其他给药途径,原则上均需开展 E&L 专项评估。
※注意:指南中并未明确规定应符合哪个具体地区的食品接触安全法规,理论上应结合制剂上市目标市场开展评估。尽管该思路较为合理,但由于要求不够明确,可能导致实际评估需要考虑更复杂的情形,对此存在一定担忧。
中国药企闯日本市场?GMP 合规不迷路!
法玛培明(日本 Pharma Planning)提供《GMP 省令》全文翻译、PMDA 审计翻译 + 专业咨询,懂日本法规更懂中国企业需求,欢迎随时联络!

