作为创新源泉的 PQS —— GMP 的优劣能否成为竞争力之源?
笔者:高桥大地
Lean PQS™ 论述 其三
作为创新源泉的 PQS —— GMP 的优劣能否成为竞争力之源?
在医药行业中,GMP 已被纳入各国法规,不实施 GMP 就无法开展药品生产与销售。换句话说,合规是理所当然的底线要求。因此,抛开质量层面不谈,单从商业角度看,有人会产生这样的疑问:只要在形式上满足既定标准不就足够了吗(这样投入产出比更高)?
在医药制造企业之间的竞争中,仅依靠 GMP 水平的高低来决定客户选择供应商的情况,其实是很有限的。
举例来说,如果某家供应商完全不满足 GMP 标准,或预计难以通过 GMP 检查,自然会被排除在候选名单之外。
但如果所有供应商都已充分满足 GMP 要求,情况又会如何?客户大概率会依据技术、价格等其他因素进行比较与选择。
GMP 实现制度化至今已过去半个世纪,从某种意义上说,遵守 GMP 早已成为行业标配、理所应当的事。
质量管理体系(QMS)的价值
关于这一论点,可参考一项针对 ISO 9001 的大规模研究(Levine, D. I., & Toffel, M. W. 2010)。
研究证实,获得 ISO 9001 认证的企业,与未认证企业相比,破产率更低,销售额与员工数量增长更显著,总人工成本及人均工资也更高。
这种效果在中小企业中尤为突出,表明导入 ISO 9001 能够强化企业经营资源与市场可信度,进而助力企业生存与发展。
为什么取得 ISO 9001 认证会带动销售额增长?
研究提示,认证本身更容易让企业成为合作伙伴的优选对象(即向市场发出合规可靠的信号)。
但另一项研究则发现(Benner, M. J., & Veloso, F. M. 2008):在认证已高度普及的行业中,企业再去获取认证,相比率先取得认证的企业,其带来的财务收益会明显减弱。
也就是说:
- 在遵守 GMP 尚非常规的时代与环境下,GMP 合规可以成为竞争力来源;
- 当遵守 GMP 已成为普遍常态时,它难以再成为核心竞争力。
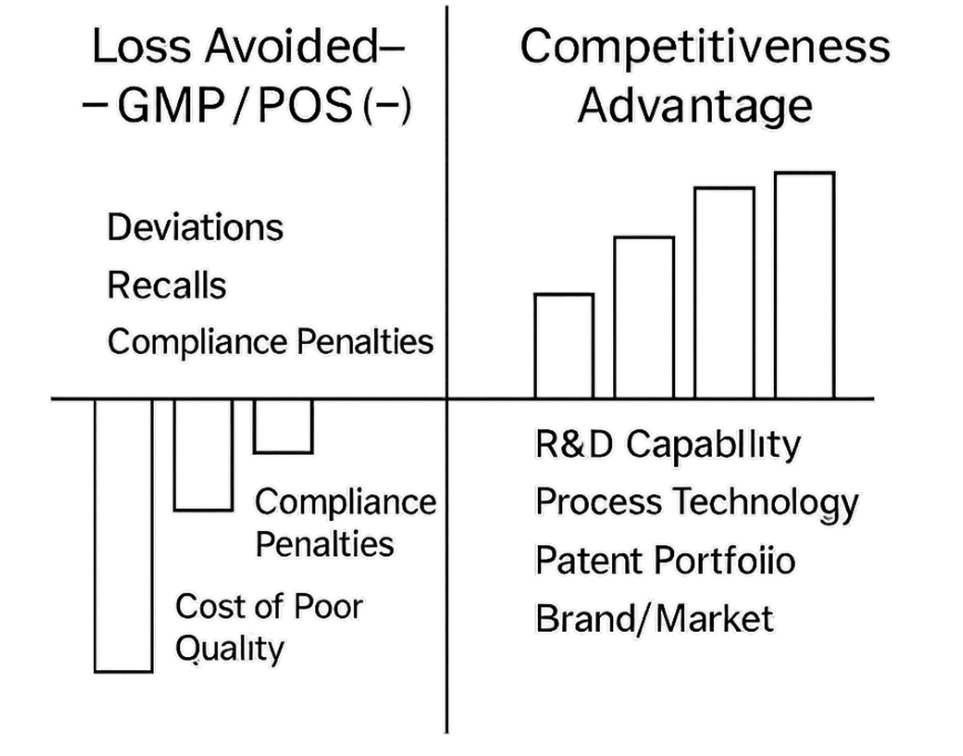
如果将构建 GMP、PQS 视为一种 “投资”,其投入产出效果该如何衡量?
GMP 与 PQS 的投入产出,往往只能从 “减少负面损失” 的角度来解释:
即实施 GMP、PQS 能够避免偏差、产品召回等各类损失,却很少能从 “创造了多少正向收益” 的角度去说明。
研发能力、技术实力、专利布局等常被视为竞争力源泉,而 GMP、PQS 却很难直接被称作企业的核心竞争力来源。
创新的源泉
但换个角度看,质量管理体系(QMS)同样可以成为创新的源泉。
有一项研究(Naveh, E., & Erez, M. 2004)基于如下假设展开:质量改进既需要严谨性(准确性、合规性、精度),也需要创新性(自主性、试验尝试、风险容忍、对新机会的响应),并探究了各类活动对不良质量成本与生产率的影响。
仅概括其结论:
在企业文化层面,可以清晰观察到 “严谨性(合规、精度)”与“创新性(试验、自主、风险容忍)”呈现不同模式。
例如,导入 ISO 9002 会显著提升严谨性,但同时会明显降低创新性。
与之相对,质量改进(QI)小组与质量目标设定则能显著提升创新性,对严谨性无额外影响。
并且,严谨性与创新性两者均分别对降低不良成本、提升生产率有显著贡献,二者并非相互对立,而是互补协同的关系。
我们可以这样理解这一结果:
QMS(延伸至 PQS)相关活动,有可能同时培育兼具严谨性与创新性的文化。
但如果在活动中只一味强调遵守规程,虽然能培养严谨性,却会削弱创新性。
因此,PQS 活动需要在遵守规程(严谨性)与优化革新规程(创新性)之间取得良好平衡。
做到这一点,PQS 就能从单纯 “减少负面损失” 的工具,升级为 “创造正向价值” 的机制,进而真正成为企业创新的源泉。
引用:
Levine, D. I., & Toffel, M. W. (2010). Quality management and job quality: How the ISO 9001 standard for quality management systems affects employees and employers (Working Paper 09-018). Harvard Business School. Forthcoming in Management Science.
Benner, M. J., & Veloso, F. M. (2008). ISO 9000 practices and financial performance: A technology coherence perspective. Journal of Operations Management, 26(5), 611–629.
Naveh, E., & Erez, M. (2004). Innovation and attention to detail in the quality improvement paradigm. Management Science, 50(11), 1576–1586.
法玛培明(日本 Pharma Planning)提供《GMP 省令》全文翻译、PMDA 审计翻译 + 专业咨询,懂日本法规更懂中国企业需求,欢迎随时联络!

